-
Un protéasome est un complexe enzymatique multiprotéique en forme de baril qui dégrade en présence d'ATP des protéines en des polypeptides plus courts et en acides aminés. Le protéasome possède une cavité en son centre, fournissant ainsi un espace clos pour la digestion des protéines, et possède des ouvertures aux deux extrémités afin de permettre l'entrée de la protéine ciblée.
La destruction via le protéasome peut être déclenchée par des phénomènes d'ubiquination. Cette ubiquination est l'un des signaux de destruction des protéines par le protéasome. La régulation du protéasome fait l'objet de recherches intensives.




http://fr.wikipedia.org/wiki/Prot%C3%A9asome
http://biology.plosjournals.org/perlserv/?request=get-document&doi=10.1371/journal.pbio.0020013
animation : http://www.avernes.fr/Oncologie/breve.php3?id_breve=49
 votre commentaire
votre commentaire
-
Il existe trois systèmes de protéolyse (destruction des protéines) :
* une destruction par des enzymes (protéases) digestives non spécifiques : trypsine, pepsine, chymotrypsine des protides alimentaires ;
http://fr.wikipedia.org/wiki/Ubiquitine
* le système lysosomial, non spécifique, permettant la dégradation et le recyclage des protéines cellulaires par des protéases intra-cellulaires ;
* le système ubiquitine-protéasome, toujours intra-cellulaire, mais cette fois hautement spécifique par un système de marquage des protéines à dégrader.
 votre commentaire
votre commentaire
-
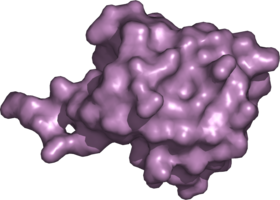

L'ubiquitine comporte 76 acides aminés et a une masse moléculaire d'environ 8500 Da. Sa structure est très conservée parmi les différentes espèces d'eucaryotes : l'ubiquitine humaine et celle d'une levure partagent 96 % d'identité pour leur séquence protéique. L'Ubiguitine est une protéine servant, elle-même, de marqueur de protéines à éliminer.
L'ubiquitination désigne la fixation spécifique et régulée d'ubiquitine sur une protéine cible. Ceci a pour conséquence la reconnaissance puis la destruction de la protéine marquée par le complexe protéolytique du protéasome. L'ubiquitine est une petite protéine présente dans toutes les cellules des eucaryotes. Sa fonction principale est de marquer d'autres protéines en vue de leur destruction, que l'on appelle la protéolyse. Plusieurs molécules d'ubiquitine sont liées de façon covalente à la protéine cible (polyubiquitination), grâce à l'action de trois enzymes, E1, E2 et E3-ligases. La protéine ainsi modifiée est ensuite dirigée vers un protéasome, une structure en forme de baril dont l'activité est régulée par l'ubiquitine, et dans laquelle la protéolyse se déroule. L'ubiquitine est alors libérée de son substrat et peut être réutilisée.
E1 (enzyme d'activation de l'ubiquitine) serait unique. Il existerait près d'une centaine de types d'E2 (enzyme de conjugaison d'ubiquitine) et plus de 1000 types d'E3 (ligase ubiquitine-protéine), cette dernière expliquant la spécificité de la réaction.
L'ubiquitine peut également marquer des protéines transmembranaires (par exemple, des récepteurs) pour les ôter de la membrane. votre commentaire
votre commentaire
Mon petit cahier de sciences naturelles










