-
 Symptômes cliniques du
Symptômes cliniques du
mutant homozygote staggerer
Cet animal présente un syndrome ataxique grave (du grec ataxia
: désordre). Le nom de ce mutant vient du mot anglais stagger
qui signifie chanceler, tituber. En effet, dès son huitième
jour, le souriceau mutant staggerer est très hésitant dans
sa démarche, avec une tendance à tituber et à traîner
les pattes.
Symptômes cliniques
du mutant homozygote reeler
Comme le mutant staggerer, le mutant reeler est très ataxique
(le verbe reel, en anglais, signifie tituber, chanceler). Les mouvements
n'atteignent pas leur but bien que leur force soit normale. L'animal est
tremblant et a un comportement d'évitement pour réaliser
certaines tâches.
Rôle de la protéine
ROR alphaLa protéine ROR alpha fait partie de la
superfamille des récepteurs nucléaires qui comprend, outre
les récepteurs des hormones thyroïdiennes et stéroïdiennes
et les dérivés des vitamines A et D, des récepteurs
nucléaires dont les ligands demeurent inconnus. De manière
générale, le mécanisme d'action des récepteurs
nucléaires est le même pour tous les membres de cette superfamille.Ces récepteurs sont des facteurs de transcription
qui se lient à l'ADN et modulent spécifiquement la transcription
de certains gènes. La protéine ROR alpha est fortement exprimée
dans les cellules de Purkinje durant le développement post-natal
du cervelet.http://www.inrp.fr/Acces/biotic/gpe/dossiers/mutcer/html/RORalpha.htm
L'absence de fonctionnalité de la protéine RORalpha pourrait
modifier les interactions avec d'autres protéines, notamment les
récepteurs nucléaires des hormones thyroïdiennes qui
jouent un rôle aussi bien dans le développement du système
nerveux que la différenciation des cellules de Purkinjie.Compte tenu du rôle central que joue cette cellule dans le réseau
synaptique cortical cérébelleux (de nombreuses fibres excitatrices
et inhibitrices sont connectées aux dendrites de cette cellule et
son axone représente la seule efférence du cortex cérébelleux),
on comprend aisément que son absence et/ou l'atrophie de l'arbre
dendritique des cellules de Purkinjie survivantes pourrait être à
l'origine d'un développement anormal du cervelet, d'où le
comportement ataxique observé, le cervelet étant impliqué
dans la gestion de la précision des mouvements.
Les phénotypes des mutants cerebelleux staggerer et reeler sont
très semblables d'un point de vue clinique et macroscopique (ataxie,
atrophie du cervelet...), mais pas au niveau cellulaire
ou moléculaire.
Ce ne sont pas les mêmes gènes qui sont
en cause dans les deux cas (gène ROR alpha pour le mutant staggerer,
gène rellin pour le mutant reeeler). Un même phénotype
clinique et macroscopique peut donc résulter de gènes différents.
http://www.inrp.fr/Acces/biotic/gpe/dossiers/mutcer/html/demarche.htm
 votre commentaire
votre commentaire
-
III- Développement du cortex cérébral
1 - Chez la souris normale
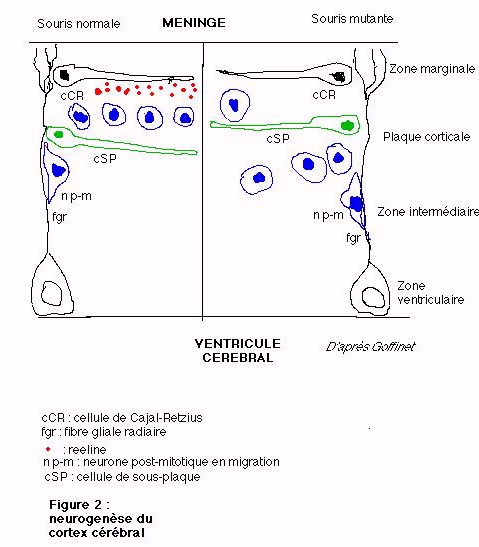
Dès le stade fœtale, une préplaque
corticale composée des premiers neurones postmitotiques engendrée
au sein des zones ventriculaires, se met en place. Ces cellules migrent
ensuite le long de fibres gliales radiaires, jusqu'à la surface
méningée et deviennent soit des cellules de Cajal-Retzius
(cCR) soit des cellules de la sous-plaque (SP). La plupart de ces cellules
disparaîtront lorsque les neurones de la plaque corticale se mettront
en place entre la couche des cCR (désormais située dans la
zone marginale) et de la SP. Enfin la plaque corticale se transformera
en substance grise du cortex définitif (décrite au dessus).La neurogenèse de la plaque corticale se
réalise donc selon un gradient intéro-externe de migration
amenant les derniers neurones formés dans les zones ventriculaires
à occuper toujours au terme de leur migration, l'interface entre
la couche marginale et la plaque corticale. Le développement de
cette plaque est très important car il est à l'origine des
six couches du cortex mature; la zone ventriculaire ne constituant plus
à la fin des processus de corticogenèse qu'une couche unique
de cellules épendymaires qui limite les ventricules cérébraux.La reeline, protéine extracellulaire sécrétée
par les cCR est déterminante dans la mise en place des couches de
neurones juxtaposés selon ce gradient intéro-externe. Ce
rôle dans la corticogenèse pourrait être une action
répulsive, empêchant les neurones en migration de pénétrer
dans la zone marginale riche en reeline respectant ainsi la stratification
normale du cortex mature (figure 2). Malgré le rôle essentiel
de cette protéine dans la corticogenèse, elle n'est qu'un
maillon important de la cascade des interactions moléculaires présidant
à la mise en place des couches corticales.2 - Chez la souris homozygote reeler
Chez l'embryon de la souris homozygote reeler,
la migration des neurones se déroule normalement jusqu'au moment
où ceux-ci arrivent près de leur destination. La reeline
n'étant pas sécrétée dans la matrice extracellulaire
par les cellules de Cajal-Retzius, le gradient répulsif vis-à-vis
des neurones de la plaque corticale n'a pas lieu si bien que les cellules
de la sous-plaque sont comme repoussées vers l'extérieur
(figure 2) en dehors de la plaque corticale sous-jacent très désorganisée.
Cela se traduit chez l'animal très précocement par un cortex
où les couches sont peu apparentes (figure 1b) : la plaque corticale
ne s'intercale plus dans la préplaque et le gradient de mise en
place des neurones pyramidaux se fait de manière quasiment inversée
c'est-à-dire selon un gradient extéro-interne.Remarque : dans des
zones cérébrales où la reeline est très exprimée
chez la souris normale, son absence chez le mutant reeler n'entraîne
pas de perturbation importante, c'est notamment le cas pour le bulbe olfactif
mais pas pour le cervelet (voir ci-dessous).IV - Développement du cortex cérébelleux
1 - Chez la souris normale
Dans le cortex cérébelleux, le rôle
joué par les cellules de Cajal-Retzius dans le cortex cérébral
en formation, serait joué par les cellules granulaires externes.
En effet, ces cellules sécréteraient la reeline dans la matrice
extracellulaire qui aurait un rôle répulsif dans la zone marginale
repoussant la plaque des cellules de Purkinje à l'interface de la
couche moléculaire et de la couche granulaire.2 - Chez le mutant homozygote reeler
Dans le cortex cérébelleux où
la reeline est pourtant peu exprimée, la modification de la séquence
nucléotidique de cette protéine entraîne de grandes
perturbation dans l'organisation du cortex cérébelleux chez
le mutant homozygote. Chez ce mutant, les cellules de Purkinje sont disposées
de manière aléatoire vraisemblablement à cause d'un
arrêt de leur migration si bien que le cervelet paraît constitué
de l'emboîtement de deux structures : à l'extérieur,
un cortex cérébelleux dont l'architecture est semblable à
celle que l'on trouve chez l'animal normal mais très mince et à
l'intérieur une masse cellulaire comportant la plupart des cellules
de Purkinje mélangées aux cellules des noyaux profonds. Faire
un renvoi vers les photos et la synthèse correspondant à
cette partie.3 - Chez d'autres mutants cérébelleux
Les précurseurs des cellules granulaires
du cortex cérébelleux, localisés dans la couche moléculaire
superficielle, mettent d'abord en place leurs axones (futures fibres parallèles)
avant que leurs corps cellulaires ne migre vers leur position définitive
dans la couche granulaire où elles contacteront les fibres moussues.Chez la souris mutante weaver (qui comme le reeler
et le staggerer présente des modifications du phénotype à
l'échelle clinique et moléculaire), les cellules précurseurs
des grains meurent durant les deux premières semaines postnatales
avant qu'elles n'aient pu migrer dans la couche granulaire interne et former
leurs fibres parallèles. Secondairement à la mort cellulaire
massive des cellules précurseurs des grains, les fibres moussues
ne trouvant plus leur cible forment alors des synapses avec les cellules
de Purkinje. Cette mutation est donc à l'origine de la désorganisation
des circuits neuroniques par disparition de leur cible.Il en est de même pour le mutant homozygote
staggerer chez qui les cellules précurseurs des cellules granulaires
migrent vers la couche moléculaire mais disparaissent presque totalement
un mois après la naissance à cause de la mort de leur cible,
les cellules de Purkinje.Outre l'intérêt des mutants cérébelleux
dans la diversité des phénotypes, ces trois mutants (staggerer,
weaver et reeler) sont à l'état homozygote de bons modèles
pour étudier l'implication du génotype dans la mise en place
des réseaux neuroniques et par voie de conséquence du fonctionnement
du système nerveux.
http://www.inrp.fr/Acces/biotic/gpe/dossiers/mutcer/html/neurogenese.htm
 votre commentaire
votre commentaire
-

Réponse intracellulaire à l'insuline et aux nutriments.
La fixation de l'insuline ou d'un IGF (Insulin-like Growth Factor) induit une cascade d'évènements qui vont conduire à l'activation de PKB. La fonction de PDK1 est d'activer des kinases telles que PKB et S6K, par phosphorylation de leur domaine catalytique.
L'activité de S6K dépend également de TOR qui joue un rôle pivot dans la réponse aux nutriments.
Les suppresseurs de tumeurs PTEN et le complexe TSC1/TSC2 sont des régulateurs négatifs de la croissance.
Les liens moléculaires entre ces voies de transduction sont controversés et mal compris. Les résultats montrant que PKB induirait la dégradation de TSC2, sont également controversés.http://www.cgm.cnrs-gif.fr/montagne/index.html
 votre commentaire
votre commentaire
Mon petit cahier de sciences naturelles



